|
Nguồn tin khởi phát về vụ thuốc giả nêu trên do Sở Y tế tỉnh Thanh Hoá cung cấp từ năm 2023. Đến tháng 8 và tháng 11/2024, Trung tâm Kiểm nghiệm Thanh Hóa thuộc Sở Y tế Tỉnh đã lấy mẫu và phát hiện 2 loại thuốc Cefuroxim 500mg và Cefixim 200mg không đạt yêu cầu định tính, nghi ngờ là thuốc giả. Thông tin này lập tức được chuyển đến cơ quan công an để điều tra.
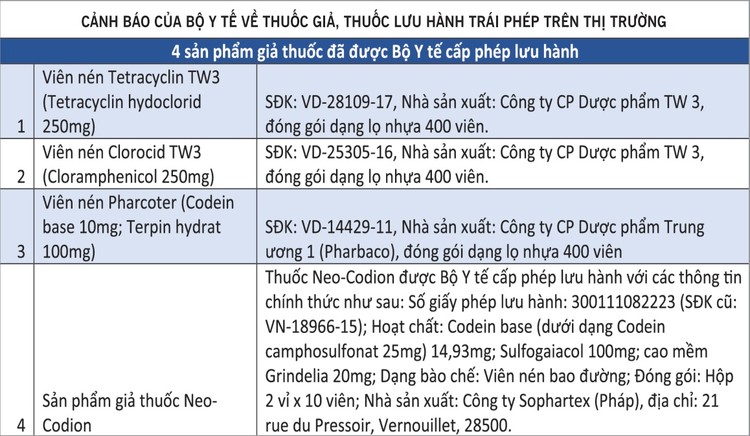
Nhờ những manh mối ban đầu này, Công an tỉnh Thanh Hóa đã triệt phá đường dây sản xuất thuốc giả quy mô lớn với tổng khối lượng lên đến 10 tấn, thu lời bất chính gần 200 tỷ đồng. Cụ thể, 20 loại thuốc giả được sản xuất tại Hà Nội, TP.HCM và An Giang. Trong đó, có 4 loại giả thuốc tân dược (44 hộp Tetracyclin, 40 hộp Clorocid, 49 hộp Pharcoter, 52 hộp Neo-Codion); 39.323 hộp gồm 16 loại sản phẩm giả nghi là thuốc đông dược, sản phẩm có nhãn ghi mục đích sử dụng như thuốc chữa bệnh.
Liên quan đến 2 sản phẩm Tetracyclin và Clorocid trong danh sách nêu trên, Công ty CP Dược phẩm Trung ương 3 đã có Văn bản số 618/TW3-TB ngày 21/4/2025 khẳng định: “Từ ngày 1/1/2021 đến nay, Công ty không sản xuất lô nào với 2 sản phẩm thuốc trên. Việc xuất hiện 2 sản phẩm viên nén Tetracyclin TW3 (Tetracyclin hydoclorid 250mg) và thuốc viên nén Clorocid TW3 (Cloramphenicol 250mg) là hàng giả và không phải do Công ty sản xuất”.
Vụ việc làm dấy lên mối lo ngại thuốc giả có thể thâm nhập vào bệnh viện, nhà thuốc bệnh viện. Trước đó, vụ án Công ty VN Pharma nhập thuốc chữa bệnh ung thư giả H-Capita 500mg diễn ra từ năm 2012 - 2013 và kết thúc vào tháng 5/2020 từng gây chấn động ngành y tế và dư luận.
Một chuyên gia mua sắm ngành y tế cho biết, quy trình lựa chọn nhà thầu cung ứng thuốc hiện nay khá chặt chẽ, nên khả năng thuốc giả trúng thầu thâm nhập vào bệnh viện công, nhà thuốc bệnh viện là rất thấp. Bởi để tham dự thầu cung ứng thuốc vào bệnh viện công, nhà thuốc bệnh viện, nhà thầu phải cung cấp đầy đủ các giấy tờ, tài liệu hợp lệ (bao gồm cả yêu cầu đối chiếu bản gốc) như: giấy đăng ký lưu hành, hóa đơn, chứng từ, nguồn gốc xuất xứ… Nếu là nhóm thuốc sản xuất trong nước thì đa số nhà thầu trúng thầu là các doanh nghiệp sản xuất có uy tín. Nếu là nhóm thuốc nhập khẩu như thuốc biệt dược gốc thì đa số được phân phối bởi các công ty lớn.
Tuy vậy, theo vị chuyên gia này, cũng không thể loại trừ hoàn toàn khả năng thuốc giả “lọt lưới” vào bệnh viện, đây vẫn là nỗi lo thường trực. “Thực tế, thuốc trúng thầu thường được cung ứng thành nhiều đợt. Mỗi bệnh viện có từ vài trăm đến vài nghìn loại thuốc, kiểm từng loại thuốc thì không xuể và cũng khó chính xác, khó nhận biết đâu là thuốc thật, đâu là thuốc giả. Chưa kể nhiều loại giấy tờ cũng dễ làm giả”, vị chuyên gia chia sẻ.
Ngay sau khi phát hiện đường dây thuốc giả nêu trên, ngày 17/4/2025, Thủ tướng Chính phủ đã ra Công điện số 41/CĐ-TTg, trong đó chỉ đạo Bộ Y tế đẩy mạnh kiểm tra, thanh tra việc chấp hành pháp luật về dược; tăng cường các biện pháp quản lý cơ sở bán buôn, bán lẻ thuốc gắn với yêu cầu kết nối cơ sở cung ứng thuốc; chỉ được mua bán các loại thuốc được cấp giấy đăng ký lưu hành, có hóa đơn, chứng từ, nguồn gốc xuất xứ đúng quy định; thực hiện việc bán thuốc theo đơn; xử lý nghiêm các trường hợp vi phạm…
Thực hiện Công điện số 41/CĐ-TTg, Bộ Y tế đã có nhiều văn bản (Văn bản số 2352/BYT-QLD ngày 20/4/2025, Văn bản số 2350/BYT-QLD ngày 20/4/2025…) đề nghị các địa phương chỉ đạo các cơ quan chức năng trên địa bàn (Ban chỉ đạo 389 địa phương, công an, quản lý thị trường, sở y tế…) mở đợt cao điểm đấu tranh phòng chống thuốc giả, thực phẩm bảo vệ sức khỏe giả; thuốc, sản phẩm bảo vệ sức khỏe không rõ nguồn gốc, không đạt chất lượng.
Đặc biệt, Bộ Y tế đề nghị các địa phương chỉ đạo các bệnh viện, cơ sở khám chữa bệnh trên địa bàn rà soát lại quy trình mua thuốc, cung ứng thuốc và tình hình cung ứng thuốc trong thời gian qua; bảo đảm thuốc được cung ứng là thuốc đã được cấp giấy phép lưu hành và cung ứng bởi các cơ sở kinh doanh dược hợp pháp, có hóa đơn chứng từ đầy đủ. Trường hợp phát hiện thuốc có dấu hiệu nghi ngờ bất thường, thuốc chưa được cấp phép lưu hành, lập tức niêm phong, không tiếp tục sử dụng, báo cáo cơ quan quản lý y tế, cơ quan chức năng để kiểm tra, xác minh và xử lý theo quy định của pháp luật.
Theo cán bộ thuộc Sở Y tế tỉnh Hậu Giang, thực hiện quy định hiện hành, hàng năm, Trung tâm Kiểm nghiệm Tỉnh sẽ lấy mẫu ngẫu nhiên từ 20 - 30 loại thuốc trúng thầu đưa vào sử dụng tại bệnh viện để kiểm tra chất lượng thuốc lưu hành trên địa bàn. Giải pháp này cần được tăng cường trong thời gian tới để ngăn chặn nguy cơ thuốc bị làm giả hoặc kém chất lượng. Manh mối của vụ án thuốc giả trên cũng xuất phát từ kết quả kiểm tra của Trung tâm Kiểm nghiệm tỉnh Thanh Hóa.
Bên cạnh trách nhiệm của các cơ quan quản lý nhà nước, nhiều ý kiến cho rằng, vai trò của cộng đồng doanh nghiệp, nhà thầu cũng rất lớn. Thực tế công tác tổ chức lựa chọn nhà thầu thời gian qua cho thấy, do cạnh tranh gắt gao, hễ thuốc nào được xếp hạng 1 mà có giá thấp bất thường thì luôn nhận được kiến nghị của các nhà thầu. Nếu là mặt hàng do mình sản xuất mà được chào giá thấp bất thường, thì chính nhà sản xuất hoặc nhà phân phối sẽ kiến nghị chủ đầu tư, bên mời thầu xem xét kỹ nguồn gốc xuất xứ của mặt hàng. Sự giám sát lẫn nhau giữa các bên được xem là một giải pháp hiệu quả để phòng chống thuốc giả trúng thầu.